 |
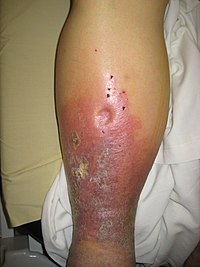
| Fig.1. Edema en miembro inferior |
El edema
es el exceso de líquido intersticial en los tejidos (Fig.1). Puede formarse por el
desequilibrio en alguno de los factores que controlan el movimiento del agua
entre el compartimiento vascular y los espacios tisulares. Esto puede ocurrir
por el aumento desproporcionado en la presión del líquido capilar
(permeabilidad), la disminución de la presión coloidosmótica capilar o la
alteración del flujo linfático.
El edema
es una manifestación de una alteración de la función fisiológica y puede
ocurrir tanto en personas sanas como enfermas. Cuando hace calor, los vasos
sanguíneos superficiales se dilatan y aumenta la retención de agua y sodio, lo
cual genera edema en las manos y los pies. El edema en los tobillos y los pies
es más pronunciado cuando el individuo permanece de pie por periodos
prolongados, porque la fuerza de gravedad se superpone con la vasodilatación
inducida por el calor y el aumento del volumen del líquido extracelular.
El edema
de pulmón que se desarrolla cuando hay un deterioro en el ventrículo izquierdo,
pone en riesgo la vida.
PATOGENIA
La
cantidad de sal y agua en el organismo depende de la ingerida y la excretada
por los riñones. Su distribución en el organismo depende del manejo interno, de
acuerdo con fuerzas físicas que actúan entre los diversos compartimientos. El
edema generalizado constituye una alteración del balance, su presencia indica
anormalidad de los mecanismos de los que depende la distribución y el acúmulo
de sales y agua en el organismo. Los mecanismos son:
- Equilibrio de las fuerzas tensionales entre el capilar y el tejido, postulados por Starling como necesarias para un intercambio hidrosalino. A este nivel, se necesita un balance correcto de las presiones hidrostática y oncótica, intra y extravasculares, para evitar que el líquido intravascular salga al intersticio.
- Función renal reguladora de la "homeostasis" en la retención y excreción de agua y sal. Esta función depende de factores hemodinámicos, hormonales, nerviosos, enzimáticos, etc.
Cualquier desequilibrio de estos mecanismos genera edema.
- Equilibrio vásculo tisular (Starling) como factor de edema.
A nivel capilar hay trasudación del líquido hemático hacia el intersticio, en el lado arterial y una reentrada del mismo hacia el vaso, en el lado venoso. La presión hidrostática del lado arteriolar es de 35mmHg, tiende a sacar líquido pero se contrarresta por la presión oncótica del plasma que es de 25mmHg. A nivel venular, la hidrostática cae a 15mmHg, sin que lo haga la oncótica y hay reabsorción. Si hay un desequilibrio de estas presiones se produce edema.
En condicionas anormales:
Hay padecimientos que alteran estas fuerzas, son aquellos que trastornan la presión hidrostática y la oncótica. Como los siguientes:
- Síndrome nefrótico o hipoalbuminemias: La presión oncótica vascular disminuye, por lo que hay trasudación del líquido vascular.
- Cirrosis portal: La trasudación puede deberse a hipertensión de arteriales de la arteria hepática y venosas de la vena porta, lo que aumenta la presión hidrostática vascular, unido a que hay una disminución de la presión oncótica por hipoalbuminemia causada por insuficiencia hepática. También puede ser por la obstrucción linfática local.
- Insuficiencia cardiaca global: Produce alteraciones en la presión hidrostática vascular.
- Obstrucciones al retorno venoso: Puede ser por taponamiento pericárdico, pericarditis constrictiva, obstrucción de la vena cava superior, etc. Puede causar edema generalizado. La hipertensión venosa explica el desequilibrio de las fuerzas de Starling.
- Nefropatías agudas o crónicas: La hipervolemia por retención renal puede trastornar estas fuerzas y producir trasudación.
- Función renal como factor de edema
El volumen y equilibrio de agua y electrolitos, depende de lo ingerido y lo excretado. El riñón mediante su función excretora regula el medio interno.
La regulación renal del balance de sodio, que es el ión básico del líquido extracelular, y de agua, depende de factores hemodinámicos, hormonales o enzimáticos.
La filtración glomerular de sodio es de 120 ml por minuto, de eso se absorbe el 99% . La reabsorción se hace como mecanismo activo que implica trabajo celular tubular y gasto energético en el túbulo proximal. La excreción renal de sal y agua depende de la cantidad de flujo sanguíneo renal, integridad de los sistemas hormonales reflejos y regulación mediante aldosterona y hormona antidiurética. También va a depender de la capacidad y grado de filtración glomerular, permeabilidad anatómica vascular, corto circuitos intrarenales, etc.
El balance intraorgánico de agua y sodio depende de la relación ingestión-excreción y su distribución en el organismo, depende de las fuerzas de Starling.
Hay patologías edematógenas en donde se ha visto que el riñón de todos los enfermos retiene cantidades altas de sal y con ello de agua. Es por eso que en todo edema generalizado hay insuficiencia renal, al menos en lo que se refiera a la excreción de sal. Este trastorno renal se deberá, a veces, a un trastorno anatómico, como en ciertas nefropatías, y en otras a un factor funcional con riñón sano, como en la insuficiencia cardiaca, cirrosis, hiperaldosteronismo, padecimientos de gasto cardiaco aumentado (hipervolémicos), etc.
Si el edema es discreto, localizado, generalmente a nivel de los tobillos y sólo ocasional, suele deberse a trastornos hidrostáticos a nivel de las venas por insuficiencia venosa, vasodilatación por calor, etc.
Anasarca: Edemas importantes y generalizados (Fig. 2), se puede agregar presencia de trasudados en cavidades serosas.
 |
| Fig. 2. Anasarca |
SEMIOLOGÍA
Para valorar el edema, es muy útil el signo de la fóvea o godete.(Fig. 3). Cuando el edema es general (acumulación de 3 a 5 litros), las zonas en declive son las primeras que registran acumulación líquida. Se toman en cuenta los siguientes aspectos:
 |
| Fig.3 Signo de godete |
- Distribución corporal: Simetría o asimetría y localización inicial.
- Coloración de la piel
- Registro de su temperatura
- Aspecto de la piel
- Coexistencia de dolor
- Consistencia (duro en los casos crónicos)
- Hallazgo de la patología cutánea en la misma zona
- Ritmo de su aparición y magnitud
- Vinculación con los movimientos o la posición
- Asociación de su aparición con algún evento externo
- Concomitancia de su enfermedad con síntomas o signos de enfermedad o situaciones fisiológicas.
Con los datos obtenidos mediante estos puntos, podemos reconocer la etiología del edema y basarnos en la patología que lo está generando, hay algunos edemas que se presentan de forma intermitente, generalmente vespertino, que mejora con el reposo nocturno, que empeora en sitio cálido, se acompaña de insomnio, irritabilidad, nicturia, parestesias, etc. Este tipo de edema aparece tanto en la menopausia como en el ciclo menstrual.
Bibliografía
- JOSE BAEZ VILLASEÑOR, JOSE LUIS BRAVO LL. IGNACIO CHAVEZ RIVERA, JORGE ESPINO VELA, HORACIO JINICH, JORGE OCARANZA M. CARLOS OCEGUERA NAVARRO. (1970). Nosología Básica Integral . México D.F. : MENDEZ OTEO.




